Allas / uima-allas / Getty Images
Tärkeimmät takeaways
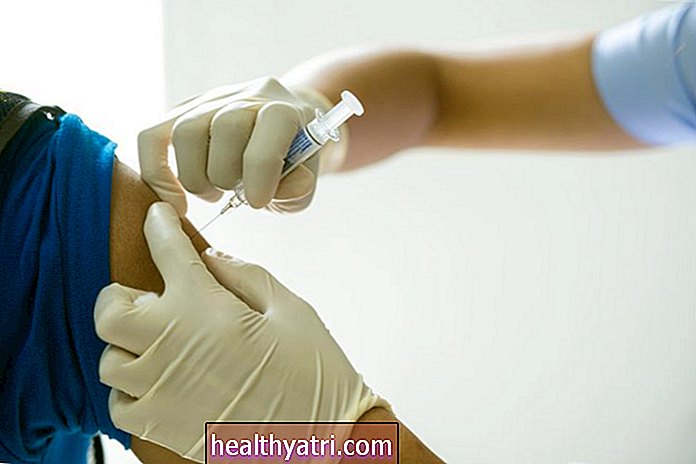
- FDA myönsi hätäkäyttövaltuuden Pfizerin ja BioNTechin kehittämälle COVID-19-rokotteelle.
- Uutiset tulevat päivää sen jälkeen, kun FDA: n neuvoa-antava komitea suositteli virastolle luvan rokotteen myöntämiseen
- Komitean tarkastelemien tietojen mukaan rokote oli 95% tehokas.
- Rokotteet voidaan jakaa 24 tunnin kuluessa myyntiluvan myöntämisestä.
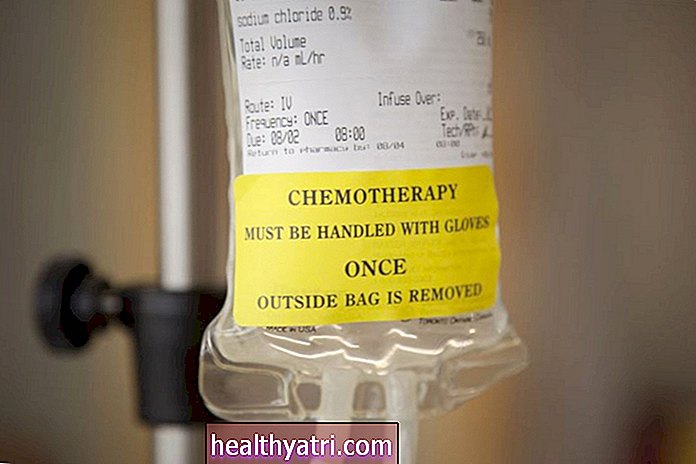
Elintarvike- ja lääkevirasto (FDA) myönsi perjantai-iltana ensimmäiselle COVID-19-rokotteelle kiireellisen käytön luvan. Pfizer Inc.:n ja saksalaisen BioNTech-yhtiön kehittämä rokote alkaa levittää pian.
Uutiset seuraavat torstaina odotettua julkista kuulemistilaisuutta, jonka aikana FDA: n neuvoa-antava paneeli äänesti 17: 4 Pfizer-rokotteen luvan puolesta yhden tyhjää.
Pfizer esitti tietoja kliinisistä tutkimuksista, joihin osallistui 43 000 aikuista osallistujaa. Aikaisemmin tällä viikolla FDA jakoi osan näistä tiedoista, mukaan lukien se, että 95% kliinisessä tutkimuksessa rokotteen saaneista ihmisistä ei kehittänyt COVID: ää -19. Haittavaikutukset olivat vähäisiä, mukaan lukien vilunväristykset, lievä kipu ja punoitus pistoskohdassa.
Hätäkäyttölupa (EUA) koskee 16-vuotiaita ja sitä vanhempia. Pfizer suorittaa myös kliinisiä tutkimuksia rokotteen turvallisuudesta ja tehosta alle 12-vuotiailla lapsilla, ja sen odotetaan lisäävän kokeita myös nuoremmille lapsille.
Turvallisuus- ja tehokkuustietoja yhä useammilta väestöiltä tarvitaan vielä
FDA: n neuvoa-antava paneeli, nimeltään Rokotteet ja niihin liittyvät biologisten tuotteiden neuvoa-antava komitea (VRBPAC), suosittelee Pfizerin toteuttavan lisätoimenpiteitä varmistaakseen, että sen rokote on turvallinen ja tehokas useammalle väestölle. Paneeli neuvoo enemmän värejä lisäämään meneillään oleviin kliinisiin kokeisiin. Värilliset ihmiset ovat todennäköisemmin kuin valkoiset saaneet sekä COVID-19: n että kuolemaan virukseen.
Paneeli keskusteli myös kahdesta raportoidusta allergisista reaktioista ihmisillä, jotka saivat rokotetta Isossa-Britanniassa tällä viikolla, jossa se on jo hyväksytty. Philadelphian lastensairaalan rokotuskoulutuskeskuksen johtaja Paul Offit kysyi Pfizerin esittäjiltä allergisista reaktioista huolissaan siitä, että vakavia allergioita sairastavat voivat päättää olla ottamatta rokotetta. Offit suositteli, että rokotteesta tehdään myös tutkimuksia ihmisillä, joilla on yleisiä allergioita.
Iso-Britannia suosittelee, että ihmiset, joilla on ollut anafylaksia lääkkeessä tai elintarvikkeessa, eivät saa rokotetta. Yhdysvallat voi lisätä samanlaisen varoituksen rinnakkain luvalla. FDA: n henkilöstö kokouksessa kertoi paneelille, että he tekivät jo kirjallisia asiakirjoja kuluttajille rokotteen turvallisuudesta ja tehokkuudesta.
Mitä tämä tarkoittaa sinulle
Elintarvike- ja lääkevirasto voi hyväksyä sen käytön muutamassa päivässä neuvoa-antavan komitean suosituksen perusteella Pfizerin COVID-19-rokotteen hyväksymiseksi. Jakelu voi alkaa hyvin pian sen jälkeen.Ensimmäisten rokoteannosten odotetaan annettavan terveydenhuollon työntekijöille ja hoitokodin asukkaille.
VRBPAC-päätöksen jälkeen FDA: n komission jäsen Stephen M.Hahn antoi lausunnon:
”Normaalisti kymmenillä tuhansilla ihmisillä tutkittujen rokotteiden tarkistusprosessi kestää kuukausia. Vaikka prosessia on nopeutettu tämän EUA: n tarkistuksen yhteydessä, FDA: n asiantuntija-arviointihenkilöstö on tarkastellut tuhansia sivuja teknistä tietoa [mukaan lukien] kliinisten tutkimusten tiedot, ei-kliiniset tiedot rokotteen kehityksestä laboratoriossa, ja valmistustiedot rokotteen valmistamisesta. "
Hahn, joka pyrkii todennäköisesti lieventämään kuluttajien pelkoja, lisäsi: "FDA: n henkilökunta tuntee vastuun siirtyä niin nopeasti kuin mahdollista tarkistusprosessin aikana. He tietävät kuitenkin, että heidän on suoritettava tehtävänsä kansanterveyden suojelemiseksi ja varmistaakseen, että kaikki hyväksytyt rokotteet täyttävät tiukat turvallisuus- ja tehostamisstandardimme, jotka amerikkalaiset ovat odottaneet. "
Valittu presidentti Joe Biden antoi myös lausunnon valiokunnan äänestyksen jälkeen: "Tieteen eheys johti meidät tähän pisteeseen".
FDA: n mukaan rokotteiden jakelu voi tapahtua 24 tunnin kuluessa luvan myöntämisestä.
FDA: n neuvoa-antava komitea tarkastelee toista Modernan valmistamaa toista COVID-19-rokotetta torstaina 17. joulukuuta.