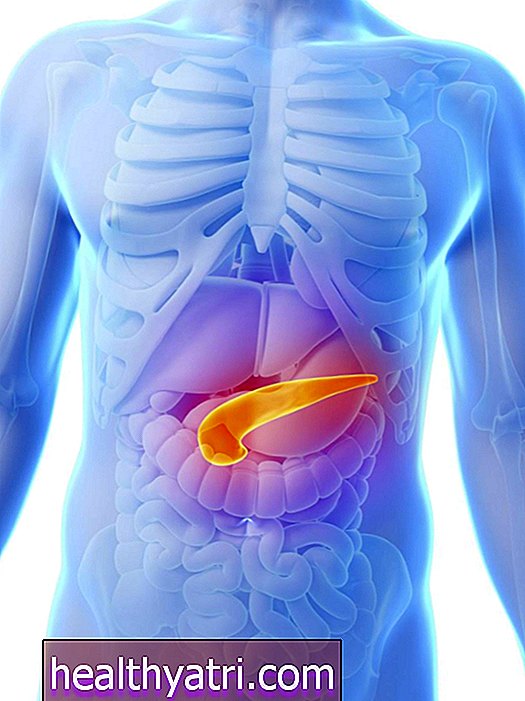
Kasvaimen agnostinen hoito viittaa syöpähoitoihin, jotka toimivat kaikissa syöpätyypeissä. Toisin sanoen, sen sijaan, että työskenneltäisiin vain yhden syöpätyypin, kuten rintasyövän, parissa, nämä hoidot voivat toimia useiden erilaisten syöpien, kuten melanooman, rintasyövän ja sarkoomien, kanssa. Lisäksi he voivat toimia sekä aikuisille että lapsille.
Panuwat Dangsungnoon / iStock
Hoitojen sijasta, jotka perustuvat kasvaimen lähtöpaikkaan, tämä hoito hoitaa syöpää, joka on peräisin mistä tahansa, kasvaimen kasvua ohjaavien erityisten molekyyliominaisuuksien perusteella. Huolimatta esiintymisestä eri kudoksissa, ei ole harvinaista, että hyvin erilaiset syöpätyypit käyttävät samaa polkua kasvamaan
Lisääntynyt tieto syövän biologiasta, kyky tehdä genomisia testejä selvittääksesi, mikä ajaa tietyn syövän kasvua, ja näille reiteille kohdennettujen lääkkeiden saatavuus on antanut tutkijoille kyvyn hoitaa monenlaisia syöpiä molekyylitasolla .
Tällä hetkellä on vain muutama lääke, joka on hyväksytty nimenomaan kasvaimen agnostiseen hoitoon, mutta sen odotetaan kasvavan nopeasti lähitulevaisuudessa. Tarkastelemme tuumorin agnostisten hoitojen määritelmää ja merkitystä, parhaillaan käytettyjä esimerkkejä sekä tämän hoitomenetelmän etuja ja rajoituksia.
Kasvaimen agnostisen hoidon määritelmä
Kasvaimen agnostinen hoito tarkoittaa lääkkeiden käyttöä syövän hoitoon kasvaimen molekyylirakenteen sijasta syövän alkuperäpaikan sijasta.
Merkitys
Syöpähoidot ovat edenneet siten, että tietyntyyppisillä syöpätyypeillä (esim. Keuhkosyöpä) hoidot valitaan jo usein kasvaimen molekyyliominaisuuksien perusteella.
Esimerkiksi ei-pienisoluisen keuhkosyövän sijaan sen sijaan, että valitsisit hoitoja ensisijaisesti mikroskoopilla nähdyn perusteella, genominen testaus (kuten seuraavan sukupolven sekvensointi) antaa lääkäreille mahdollisuuden selvittää, onko syöpällä spesifistä geenimutaatiota (tai muuta muutosta) ), johon kohdennettuja hoitoja on nyt saatavana.
Vaikka tiettyä kemoterapialääkettä voidaan antaa useammalle kuin yhdelle syöpätyypille, hoidon periaate on erilainen. Kemoterapia käsittelee olennaisesti kaikki nopeasti jakautuvat solut.
Sitä vastoin kohdennetut hoidot (ja eri tavalla immunoterapialääkkeet) kohdistavat hyvin spesifisen kasvuradan. Kaksi samantyyppistä ja -vaiheista syöpää, jotka reagoivat samalla tavalla kuin kemoterapia, voivat reagoida hyvin eri tavalla kohdennetulla lääkkeellä tapahtuvaan hoitoon.
Jos kasvain sisältää mutaation, kuten EGFR-mutaation, mutaatioon kohdistuvan lääkkeen (kuten EGFR-estäjän) käyttö johtaa todennäköisesti syövän kasvun hallintaan. Sitä vastoin, jos kasvain, jolla ei ole tätä mutaatiota, ei todennäköisesti reagoisi lainkaan EGFR-estäjään.
Hoidot, jotka kohdistuvat näihin spesifisiin genomimuutoksiin (joita kutsutaan joskus kasvaimen "molekyylimerkinnöiksi") ovat muuttaneet suuresti sekä monien syöpien hoitoa että keskittymistä lääkekehitykseen.
Biologia ja terminologia
Kasvaimen agnostisista hoidoista keskustelemiseksi on hyödyllistä puhua joistakin hämmentävästä biologiasta. Onneksi ihmisillä on enemmän valtaa ja oppia syöpäänsä, mutta se ei ole toisin kuin haastavan vieraan kielen oppiminen.
Jotta syöpä kasvaa edelleen, solujen on oltava riittävän erilaisia kuin normaalit solut, jotta ne eivät kuuntele kehon normaaleja signaaleja lopettamaan kasvunsa tai eliminoimaan itsensä. Solujen kasvuun liittyy monimutkaisia reittejä, ja poikkeavuudet useissa näistä pisteistä voivat johtaa hallitsemattomaan kasvuun.
Geenimutaatiot (ja muut muutokset) ovat syövän perusta, ja näiden mutaatioiden sarja johtaa siihen, että solusta tulee syöpäsolu. Geenit ovat proteiinien suunnitelma, ja proteiinit puolestaan ovat aineita, jotka joko stimuloivat tai estävät eri pisteitä näillä reiteillä.
Nyt on olemassa useita lääkkeitä (ja monia muita kehitys- ja kliinisissä tutkimuksissa), jotka estävät joitain näistä proteiineista ja lopettavat siten signaalin, joka johtaa syövän jatkuvaan kasvuun. Muutama termi kuulostaa hyvin hämmentävältä, mutta on melko yksinkertainen määriteltyään.
Termi kuljettajan mutaatio viittaa mutaatioon geenissä, joka koodaa proteiinia, joka kontrolloi syövän kasvua. Syöpä, jolla on tämä mutaatio (tai muu muutos), on "riippuvainen" epänormaalista proteiinista, joka on tuotettu kasvun jatkamiseksi. Onkologit käyttävät usein termiä onkogeeniriippuvuus kuvaamaan tätä käyttäytymistä.
Erityistä mutaatiota kutsutaan sitten syövän molekyyliallekirjoitukseksi.
Kriteerit kasvaimen agnostisiin hoitoihin
Jotta hoito olisi tehokasta kaikissa syöpätyypeissä, on olemassa muutamia käyttökriteerejä.
- Erityinen mutaatio (tai muu muutos) on löydettävä. Toisin sanoen testauksen on oltava käytettävissä muutoksen havaitsemiseksi ja se on tehtävä melko usein.
- Kasvainten, joilla on erityinen mutaatio, on vastattava hoitoon kohdennettuihin hoitoihin.
- Mutaatio on löydettävä monista erilaisista syöpätyypeistä.
Käyttö ja esimerkit
Tällä hetkellä on olemassa muutamia lääkkeitä, jotka on hyväksytty kasvaimen agnostiseen käyttöön, ja muita, joita käytetään merkitsemättöminä tällä tavalla. Tarkastelemme joitain näistä lääkkeistä.
Keytruda
Keytruda (pembrolitsumabi) oli ensimmäinen tuumorin agnostiseen hoitoon hyväksytty lääke vuonna 2017. Ketruda on PD-monoklonaalinen vasta-aine, joka on luokiteltu tarkistuspisteen inhitiboriksi (eräänlainen immunoterapialääke). Se toimii olennaisesti "poistamalla jarrut". kehon oman immuunijärjestelmän vaste syöpään.
Keytruda on hyväksytty aikuisten tai lasten kiinteisiin tuumoreihin, joiden on havaittu olevan erittäin mikrosateliittisen epävakauden (MSI-H) tai joilla puutteita ei löydy yhteensopimattomuudesta (dMMR). Joko MSI-H tai dMMR voidaan löytää kasvaimella tehtävillä testeillä (PCR tai immunohistokemia).
Vuonna 2020 Keytruda sai toisen kasvaimen agnostisen hyväksynnän ihmisille, joilla on kiinteät kasvaimet, joilla on suuri mutaatiokuorma. Mutaatiokuorma on mittari syöpäkasvaimessa läsnä olevien mutaatioiden määrästä, ja se liittyy (mutta ei aina) positiiviseen vasteeseen immunoterapialääkkeisiin.
Vitrakvi
Vitrakvi (larotrektinibi) on toinen lääke, joka sai hyväksynnän kasvaimen agnostiseen hoitoon vuonna 2018.Se on hyväksytty aikuisille tai lapsille, joilla on kasvaimia, joissa on NTRK-fuusioproteiineja.Neurotrofisen reseptorikinaasin (NTRK) geenifuusio on vain noin 1% monista kiinteistä kasvaimista, kuten keuhkosyöpä, mutta niitä voi esiintyä jopa 60% joistakin sarkoomatyypeistä.
Joitakin syöpätyyppejä, joihin vaste on osoitettu, ovat keuhkosyöpä, melanooma, GIST-kasvaimet, paksusuolisyöpä, pehmytkudossarkoomat, sylkirauhasen kasvaimet, infantiili fibrosarkooma, rintasyöpä ja haimasyöpä.
Aikuisilla, joilla oli kasvaimia, joissa oli NTRK-geenifuusio, vasteprosentti Vitrakville oli 75-80% .Erityisessä lapsilla tehdyssä tutkimuksessa kokonaisvaste oli 90%.
Nämä vastaukset havaittiin silloinkin, kun ihmiset olivat saaneet aikaisempia hoitoja. Tämä vahvistaa, kuinka riippuvaisia tästä reitistä nämä kasvaimet ovat kasvulle. Vastausten lukumäärä ei ollut vain korkea, mutta Vitrakvin käyttäminen pystyi voittamaan joitain tapauksia, antamaan kirurgien tehdä vähemmän hämmentäviä leikkauksia lapsille.
Rozlytrek
Vuonna 2019 FDA hyväksyi Rozlytrekin (entrektinibin) käytön ihmisille, joilla on kasvaimia, joissa on NTRK-geenifuusio, sekä ei-pienisoluiselle keuhkosyövälle, jolla on ROS1-muutos.
Lääke on hyväksytty aikuisille tai lapsille, joilla on metastaattinen syöpä tai joille leikkaus voi johtaa merkittävään vääristymiseen. Arvioinnin aikana yleinen vaste oli harvinainen 78%.
Tutkimuksessa yleisimmät syövät olivat sarkooma, ei-pienisoluinen keuhkosyöpä, rintasyöpä, paksusuolen ja paksusuolisyöpä, kilpirauhassyöpä ja rintarauhasen analoginen erityssyöpä.
BRAF-mutaatiot
Vaikka spesifistä kasvaimen agnostista hoitoa ei ole hyväksytty, tutkijat ovat havainneet, että ihmiset, joilla on erilainen syöpätyyppi ja joilla on BRAF-mutaatioita, reagoivat usein BRAF-estäjien (yleensä yhdessä MEK-estäjien) hoitoon.
BRAF-mutaatiot havaittiin alun perin (ja hoidettiin) metastaattista melanoomaa sairastavilla ihmisillä, mutta nyt ne on osoitettu ei-pienisoluisessa keuhkosyövässä (noin 3%), paksusuolisyöpässä, karvassoluleukemiassa, kilpirauhassyövässä, seroosisessa munasarjasyövässä ja muissa.
Muita esimerkkejä
Koska seuraavan sukupolven testejä tehdään useammin, tutkijat alkavat nähdä geenimuutoksia, joiden on ajateltu olevan eristetty tietyntyyppisiin syöpiin.
Esimerkiksi HER2-positiivisella rintasyövällä havaittu muutos esiintyy joillakin keuhkosyöpää sairastavilla ihmisillä.Muita esimerkkejä ovat Lynparza-lääkkeen (olaparibi) käyttö paitsi rintasyövässä myös munasarjasyöpä, eturauhassyöpä ja haimasyöpä, jolla on BRCA-mutaatio.
Testaus ja kokeilut
Tällä hetkellä kehityksessä on useita lääkkeitä sekä kliinisissä tutkimuksissa. Kliinisten tutkimusten tyypit, joissa joskus arvioidaan lääkkeitä eri syöpäluokissa, ovat korikokeet ja sateenvarjo-tutkimukset. Arviointia helpottaa tarkkuusotteluprotokolla nimeltä NCI-MATCH.
Edut ja rajoitukset
On selvää hyötyä, kun on mahdollista käyttää yhtä hoitoa useille erilaisille syöpätyypeille, mutta on myös rajoituksia.
Edut
On sanomattakin selvää, että kasvaimen agnostisilla lääkkeillä on etuja lääkkeiden tutkimuksessa ja kehittämisessä. Lääkekehitys on erittäin kallista. Missä tämä lähestymistapa todella erottuu, on kuitenkin harvinaisten syöpien hoidossa.
Syöpätapauksissa, jotka vaikuttavat vain pieneen osaan väestöstä (esimerkiksi infantiili fibrosarkooma), ei välttämättä "maksa" yritykselle tutkia ja kehittää lääkitystä. Tämä ei tarkoita sitä, ettei se ole tärkeä, mutta yritykset sijoittavat rahaa tavoin, joilla he näkevät tuoton.
Kasvaimen agnostisten hoitojen avulla lääkeyritykset voivat kuitenkin saada korvausta, kun lääkkeestä hyötyy joukko ihmisiä, joilla on yleisempiä syöpiä. Esimerkiksi Vitrakvi.
Toinen vahva etu on, että tutkimus edistää syöpää ympäröivää tiedettä. Mutta tutkittaessa kasvun molekyylireittejä hoidon löytämiseksi toivotaan löytävän uusia reittejä toivomalla vielä enemmän hoitoja.
Rajoitukset / riskit
Vaikka kasvaimen agnostiset hoidot saattavat kuulostaa tulevaisuuden hoitotavoitteilta, niiden käytölle on useita rajoituksia.
Kaikki syövät eivät vastaa samaan
Vaikka kahdella erityyppisellä syövällä on sama mutaatio, joka ohjaa syövän kasvua, vaste mutaatioon kohdentavalle lääkkeelle voi olla hyvin erilainen.
Esimerkki on BRAF V600E -mutaatioista. Melanoomat tai karvaisten solujen leukemiasolut, joissa on mutaatio, ovat yleensä hyvin reagoivia lääkkeisiin, jotka estävät BRAF: ää. Sitä vastoin paksusuolen syöpät, joilla on sama mutaatio, eivät yleensä reagoi BRAF-estäjiin.
Kaksi syöpätyyppiä, joilla on sama kuljettajan mutaatio, saattavat tarvita hyvin erilaisia hoitoja kasvun hallitsemiseksi.
Toinen rajoitus on, että genomikokeista ei ole vielä tullut rutiinia kaikille ihmisille edes syöpätapauksissa, joissa tämä olisi erittäin suositeltavaa (esimerkiksi ei-pienisoluisen keuhkosyövän tapauksessa). Joillakin syöpätyypeillä, etenkin harvoin havaituilla, voi olla vain vähän tietoa läsnä olevista yhteisistä molekyyliominaisuuksista.
Useimmiten uudempien lääkkeiden, erityisesti kasvaimen agnostisten hoitojen, käyttö on saatavilla vain kliinisessä tutkimuksessa. Kliinisten tutkimusten osallistuminen ei ole vain liian matala Yhdysvalloissa, mutta osallistumisessa on merkittäviä eroja, jotka tekevät hoitojen arvioinnista iän, rodun, sukupuolen ja haastavamman
Kehittäminen vie myös aikaa. Erään tutkimuksen mukaan keskimääräinen aika huumeiden löytämisestä testaukseen ja hyväksyntään Yhdysvalloissa on 15 vuotta. Ja vaikka nämä hoidot saavuttavat edistyneen tason kliinisissä tutkimuksissa, ne voivat silti auttaa vain vähemmistöä ihmisistä.
Lopuksi, suurin osa uusista syövän hoidoista on nyt hinnoiteltu alueelle, joka ei ole kestävä.
Sana Verywelliltä
Syöpien hoito molekyylien perusteella ei ole uutta, mutta näiden hoitojen käyttämistä monissa syöpätyypeissä voidaan melkein ajatella tarkkuuslääkkeinä steroideilla.
Vaikka syövän alkuperä (histologia) pysyy tärkeänä, hoidon keskittyminen molekyyliominaisuuksiin (genomiikka ja immunologiset poikkeavuudet jne.) Lupaavat edistää onkologian alaa tavoilla, jotka voivat yllättää meitä yhtä paljon kuin kohdennetun hoidon viimeaikainen kehitys ja immunoterapia.
Samalla on jännittävää ajatella, että kasvaimen agnostinen hoito voi johtaa harvinaisten syöpien (etenkin lasten) hoitoihin, jotka muuten eivät olisi olleet mahdollisia.