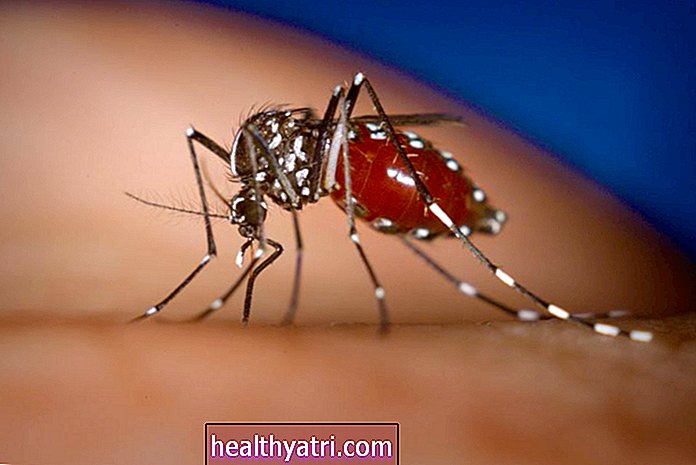
wera Rodsawang / Getty Images
Tärkeimmät takeaways
- Uudesta Messenger RNA (mRNA) -rokotteesta tuli ensimmäinen COVID-19-rokote, joka on hyväksytty hätäkäyttöön Yhdysvalloissa.
- Tutkijat kehittävät 10 erilaista rokotemallia COVID-19-rokotteiden luomiseksi
- Rokotteen on oltava vähintään 70-prosenttisesti tehokas COVID-19: n hävittämiseksi
- Rokotteen nopea jäljittäminen tarkoittaa suojatoimien ohittamista
Kilpailu turvallisen ja tehokkaan rokotteen löytämisestä COVID-19: lle (koronavirustauti 2019) ei ole ennennäkemätöntä nykyaikaisessa lääketieteellisessä historiassa. Ei AIDS-pandemian jälkeen, jos 1980- ja 90-luvuilla tutkijat, hallitukset ja yritykset kokoontuvat yhteen koordinoidusti jakamaan tietoja ja resursseja, jotka saattavat jonain päivänä johtaa täysin suojaavan rokotteen kehittämiseen.
Aids-pandemian tapaan tutkijoiden on paljon opittava viruksesta.
Mutta toivoa on. Joulukuussa 2020 Pohjois-Amerikassa, Euroopassa ja Aasiassa oli aktiivisesti kehitteillä vähintään 233 rokotekandidaattia, joiden tavoitteena oli tuoda ainakin yksi kokonaan markkinoille vuoteen 2021 mennessä.
Elintarvike- ja lääkevirasto (FDA) myönsi 11. joulukuuta Pfizerin ja BioNTechin yhdessä kehittämän COVID-19-rokotehakijan hätäkäyttövaltuuden. Tämä hätäkäyttö on hyväksytty 16-vuotiaille ja sitä vanhemmille. Toiselle Modernan COVID-19-rokotekandidaatille myönnettiin hätäkäyttölupa 18. joulukuuta. Molemmat rokotteet ovat uusia messenger RNA (mRNA) -rokotteita, joissa on immuunisolujen geneettiset ohjeet osaksi proteiinia, joka laukaisee immuunivasteen COVID: lle. -19.
Miksi tällä on merkitystä
Vaikka pelottavat haasteet saattavatkin tuntua, rokote on edelleen tehokkain tapa estää varhaiset COVID-19-pandemian määrittäneet maailmanlaajuiset lukkiutumiset ja sosiaaliset etäisyystoimenpiteet.
Tavoitteet ja haasteet
Aikajana itsessään asettaa valtavia haasteita. Ottaen huomioon, että rokotteiden kehittäminen vie keskimäärin 10,71 vuotta prekliinisen tutkimuksen alusta lopulliseen sääntelyhyväksyntään, tutkijoiden tehtävänä on tiivistää aikajanaa tavalla, jota rokotetutkimuksessa on suurelta osin tuntematon.
Jotta rokotetta voidaan pitää elinkelpoisena, sen on oltava turvallinen, edullinen, vakaa, helposti valmistettavissa tuotannossa ja annettava helposti niin monelle planeetan 7,8 miljardista ihmisestä kuin mahdollista.
Samanaikaisesti, jos rokotteen on tarkoitus lopettaa pandemia, sen tehokkuuden on oltava korkea, jopa korkeampi kuin influenssarokotteen. Kaikki muu kuin tämä voi hillitä infektioiden leviämistä, mutta ei estää niitä.
Vain 6% kehitteillä olevista rokotteista tapahtuu prekliinisestä tutkimuksesta markkinoiden vapauttamiseen.
Rokotteiden tehokkuus
Maailman terveysjärjestön (WHO) mukaan rokotteen on oltava vähintään 70-prosenttisesti tehokas populaatiosta, jotta rokote hävittäisi täydellisesti COVID-19: n ja sen tulisi tarjota kestävä suoja vähintään vuoden ajan. Tällä tasolla virus olisi vähemmän kykenevä mutaatioon, kun se siirtyy ihmiseltä toiselle, ja todennäköisemmin tuottamaan lauman immuniteetin (jossa suurilla väestönosilla kehittyy immuuniresistenssi virukselle).
Nämä vertailuarvot ovat uskomattoman kunnianhimoisia, mutta eivät mahdotonta.
60 prosentin tehokkuudella WHO väittää, että taudinpurkauksia esiintyy edelleen ja että karjan immuniteetti ei rakene riittävän aggressiivisesti pandemian lopettamiseksi.
COVID-19-rokote, jonka tehokkuus on 50%, on hyödyllinen korkean riskin yksilöille, mutta se ei estä taudinpurkauksia eikä vähennä etulinjan terveydenhuoltojärjestelmien stressiä, jos taudinpurkaus tapahtuu.
Esimerkiksi influenssarokotteen teho oli alle 45% vuosina 2019-2020 influenssakauden aikana tautien torjunnan ja ehkäisyn keskusten (CDC) mukaan. Jotkut yksittäisistä rokotekomponenteista olivat vain 37% tehokkaita.
mRNA-rokotteet COVID-19: lle
Pfizer ilmoitti 18. marraskuuta, että sen vaiheen III rokotetutkimus osoitti 95%: n tehokkuuden COVID-19: tä vastaan.Moderna ilmoitti 30. marraskuuta, että sen rokotteen vaiheen III tutkimus osoitti 94%: n tehokkuutta COVID-19: ää vastaan ja myös 100%: n tehokkuutta vakavaa tautia vastaan. Vertaisarviointi on edelleen vireillä näissä kokeissa.
Terveysviranomaiset voivat hyväksyä rokotteen, jonka tehokkuus on alle optimaalisen, jos hyödyt (erityisesti vanhuksille ja köyhille) ovat suuremmat kuin riskit.
Kustannus
Rokotetta ei voida pitää elinkelpoisena, jos se ei ole edullinen.
Toisin kuin influenssarokote, joka on massatuotettu ruiskuttamalla kananmunia viruksella, COVID-19: ää eikä sen koronaviruksen serkkuja (kuten SARS ja MERS) ei voida tuottaa munissa. Siksi tarvitaan kokonaan uutta tuotantoteknologiaa vastaamaan vuotuisen influenssarokotteen tuotantomäärää, josta yli 190 miljoonaa annosta toimitetaan Yhdysvalloissa vuosittain.
Uudet geneettiset rokotteet, mukaan lukien Pfizer-BioNTech- ja Moderna-rokotekandidaatit, kehitetään koeputkiin tai säiliöihin. Niitä ei tarvitse kasvattaa munissa tai soluissa, mikä säästää kehityksen aikaa ja kustannuksia.Vaikka tämä on ensimmäinen kerta, kun niitä tuotettaisiin massatuotantona, joten kokonaiskustannukset ja monet logistiikkatiedot ovat edelleen tuntemattomia.
Yhdysvalloilla on sopimuksia mRNA-rokotekandidaattien ostamisesta Pfizer-BioNTechiltä ja Modernalta, mutta näiden ja muiden rokotteiden kustannuksia ja saatavuutta monissa maailman maissa ei ole vielä määritelty.
Yhdysvaltain hallituksella on sopimus Pfizerin ja BioNTechin kanssa alkuperäisestä 100 miljoonan annoksen tilauksesta 1,95 miljardille dollarille ja oikeudet hankkia jopa 500 miljoonaa lisäannosta. Ne, jotka saavat rokotteen, saavat sen ilmaiseksi, ja rokote on saanut hätäkäyttöluvan myös Isossa-Britanniassa, Bahrainissa, Saudi-Arabiassa, Kanadassa ja Meksikossa.
Liittovaltion hallituksella on 1,5 miljardin dollarin sopimus Modernan kanssa 100 miljoonasta rokoteannoksesta ja mahdollisuus hankkia lisää 400 miljoonaa annosta (se on jo pyytänyt 100 miljoonaa ylimääräistä). Se auttoi myös rahoittamaan sen kehitystä 955 miljoonan dollarin sopimuksella, jolloin alkuperäinen kokonaissumma oli 2,48 miljardia dollaria. Jos se saa hätävaltuutuksen, se annetaan myös Yhdysvalloissa asuville ihmisille ilmaiseksi.
Jakelu
Kun COVID-19-rokotteet on kehitetty, seuraava haaste on jakaa ne oikeudenmukaisesti, varsinkin jos tuotantokapasiteetti on rajallinen. Tämä vaatii laajaa epidemiologista tutkimusta sen määrittämiseksi, mitkä populaatiot ovat eniten sairauden ja kuoleman vaarassa.
Näiden huolenaiheiden ohittamiseksi jotkut asiantuntijat suosittelivat, että rahoitus suunnataan kokeiltuihin ja todellisiin rokotemalleihin, jotka ovat todennäköisesti skaalautuvia, eikä kokeellisiin malleihin, jotka saattavat vaatia miljardeja dollareita rakenteellisiin investointeihin ennen kuin rokotteen ensimmäinen määrä on edes tuotettu.
Suuret investoinnit tehtiin kokeellisiin, vaikka ne asettaisivat haasteita massan jakelulle, mukaan lukien Pfizer-BioNTech -rokotteen mahdolliset kustannukset ja erittäin kylmät lämpötilavaatimukset, jotka tarvitsevat erikoistuneita pakastimia.
Pfizer ja BioNTech ennustavat maailmanlaajuisen tuotannon, joka on jopa 50 miljoonaa annosta vuonna 2020 ja jopa 1,3 miljardia annosta vuoden 2021 loppuun mennessä. Moderna arvioi noin 20 miljoonan annoksen tuotannon valmiiksi lähetettäväksi Yhdysvaltoihin vuoden loppuun mennessä. 2020 ja maailmanlaajuinen tuotanto 500–1 miljardi annosta vuonna 2021.
Eettinenongelma
Nopeasti seurattava rokote minimoi joitain tarkastuksia ja tasapainoja, jotka on suunniteltu pitämään ihmiset turvassa. Tämä ei tarkoita, että sen tekeminen on mahdotonta. Se vaatii yksinkertaisesti suurempaa valvontaa valvontaviranomaisilta, kuten WHO: lta, National Institutes of Health (NIH): lta, Euroopan lääkevirastolta (EMA) ja Kiinan elintarvike- ja lääkevirastolta (CFDA), jotta varmistetaan tutkimuksen turvallinen suorittaminen ja eettisesti.
Jopa sääntelyn valvonnassa kilpailu markkinavalmiin rokotteen tuottamisesta kahden vuoden kuluessa on herättänyt huolta etiikan asiantuntijoiden keskuudessa, jotka väittävät, ettet voi kehittää rokotetta nopeastijaturvallisesti.
"Haastetutkimuksiin" sisältyy esimerkiksi aiemmin tartuttamattomien, terveiden, nuorten aikuisten rekrytointi, jotka ovat suoraan altistuneet COVID-19: lle kandidaattirokotuksen jälkeen. Jos altistusrokote osoittautuu turvalliseksi ja tehokkaaksi tässä matalan riskin ryhmässä seuraava vaihe olisi rekrytoida korkeamman riskin aikuisia perinteiseen kaksoissokkoutettuun tutkimukseen. Vaikka tällaisia haasteita käytetään vähemmän tappavilla sairauksilla, kuten flunssa, ihmisten tahallinen altistaminen COVID-19: lle on huomattavasti riskialttiimpaa.
Kun COVID-19-tutkimus siirtyy prekliinisistä tutkimuksista suurempiin ihmiskokeisiin, tällaiset ongelmat asettavat sääntelyviranomaisille paineen päättää, mitkä riskit tällä uudella rajalla ovat "hyväksyttäviä" ja mitkä eivät.
Mistä aloittaa
Tutkijat eivät ole aloittaneet tyhjästä kehittäessään COVID-19-rokotemallejaan (alustoja). Ei ole olemassa vain tehokkaita rokotteita, jotka perustuvat vastaaviin viruksiin, mutta kokeellisia, jotka ovat osoittaneet osittaisen suojan koronaviruksia vastaan, kuten MERS ja SARS.
COVID-19 kuuluu suureen ryhmään viruksia, joita kutsutaan RNA-viruksiksi, joihin kuuluvat Ebola, hepatiitti C, HIV, influenssa, tuhkarokko, raivotauti ja monet muut tartuntataudit. Nämä on jaoteltu edelleen:
- Ryhmän IV RNA-virukset: Näitä ovat koronavirukset, hepatiittivirukset, flavivirukset (liittyvät keltakuumeeseen ja Länsi-Niilin kuumeeseen), poliovirukset ja rinovirukset (yksi monista tavallisista kylmäviruksista)
- Coronaviridae: Ryhmän IV RNA-virusten perhe, joka sisältää neljä tavalliseen kylmään liittyvää koronaviruskantaa ja kolme vakavaa hengityselinsairautta (MERS, SARS ja COVID-19).
Näiden virusten näkemys, vaikka se onkin vähäistä, voi tarjota tutkijoille todisteita, joita tarvitaan heidän alustojensa rakentamiseen ja testaamiseen. Vaikka foorumi epäonnistuu, se voi osoittaa tutkijoita elinkelpoisempien suuntaan.
Jopa monien ryhmän IV RNA-virusten joukossa on kehitetty vain kourallinen rokotteita (polio, vihurirokko, hepatiitti A, hepatiitti B) ensimmäisestä keltakuumarokotteesta vuonna 1937 lähtien. Koronaviruksia ei ole toistaiseksi rokotettu. jotka on täysin hyväksytty ja lisensoitu Yhdysvalloissa.
Rokotteiden kehittämisen mallit
Kilpailua tehokkaan COVID-19-rokotteen löytämiseksi koordinoivat suurelta osin WHO ja globaalit kumppanit, kuten äskettäin perustettu koalitiota epidemian varautumisen innovaatioiksi (CEPI). Näiden organisaatioiden tehtävänä on valvoa tutkimusympäristöä, jotta resurssit voidaan kohdistaa lupaavimpiin ehdokkaisiin.
CEPI esitteli COVID-19: n käytettävissä olevat eri alustat, joiden pohjalta jotkut ovat päivitettyjä malleja, jotka perustuvat 1950- ja 60-luvun Salk- ja Sabin-poliorokotteisiin. Toiset ovat seuraavan sukupolven rokotteita, jotka tukeutuvat geenitekniikkaan tai uusiin jakelujärjestelmiin (ns.
proteiinirokotteet
Jokaisella ehdotetulla alustalla on etuja ja haittoja. Jotkut rokotetyypeistä valmistetaan helposti tuotantomittakaavassa, mutta niiden vaste on yleisempi (ja siksi ne eivät todennäköisesti saavuta pandemian lopettamiseen tarvittavia tehokkuuden tasoja). Muut uudemmat mallit voivat saada aikaan voimakkaamman vastauksen, mutta vähän tiedetään siitä, mitä rokote voi maksaa tai voidaanko se tuottaa maailmanlaajuisesti.
CEPI: n hahmottamista 10 rokotealustasta viisi ei ole koskaan tuottanut elinkelpoista rokotetta ihmisillä. Silti jotkut (kuten DNA-rokotealusta) ovat luoneet tehokkaita rokotteita eläimille.
Rokotteiden kehittämisprosessi
Vaikka rokotteiden kehitysvaiheet pakataan, prosessi, jolla COVID-19-rokotteet hyväksytään, pysyy suunnilleen samana. Vaiheet voidaan jakaa seuraavasti:
- Prekliiniset vaiheet
- Kliininen kehitys
- Lainsäädännön tarkastelu ja hyväksyminen
- Valmistus
- Laadunvalvonta
Prekliininen vaihe on ajanjakso, jonka aikana tutkijat keräävät toteutettavuus- ja turvallisuustietoja sekä aiempien tutkimusten todisteita toimitettaviksi valtion sääntelyviranomaisille hyväksynnän testaamiseksi. Yhdysvalloissa FDA valvoo tätä prosessia. Muilla mailla tai alueilla on omat sääntelyelimet.
Kliininen kehitys on vaihe, jonka aikana varsinaista tutkimusta tehdään ihmisillä. Vaiheita on neljä:
- Vaiheen I tavoitteena on löytää paras annos, jolla on vähiten sivuvaikutuksia. Rokote testataan pienessä alle 100 osallistujaryhmässä. Noin 70% rokotteista menee tämän alkuvaiheen ohi.
- Vaihe II laajentaa testausta usealle sadalle osallistujalle turvalliseksi pidetyn annoksen perusteella. Osallistujat jaotellaan vastaamaan COVID-19-vaarassa olevien ihmisten yleistä väestötietoa. Noin kolmasosa vaiheen II ehdokkaista pääsee vaiheeseen III.
- Vaihe III sisältää tuhansia osallistujia useissa sivustoissa, jotka valitaan satunnaisesti joko saamaan todellinen rokote tai lumelääke. Nämä tutkimukset ovat tyypillisesti kaksoissokkoutettuja, jotta tutkijat eivätkä osallistujat eivät tiedä, mikä rokote annetaan. Tässä vaiheessa suurin osa rokotteista epäonnistuu.
- Vaihe IV tapahtuu rokotteen hyväksymisen jälkeen ja jatkuu useita vuosia rokotteen todellisen tehon ja turvallisuuden arvioimiseksi. Tämä vaihe tunnetaan myös nimellä "markkinoinnin jälkeinen valvonta".
COVID-19-rokotteet: Pysy ajan tasalla siitä, mitä rokotteita on saatavilla, kuka niitä saa ja kuinka turvallisia ne ovat.
Ajoitus
Niin yksinkertainen kuin prosessi onkin, rokotteen epäonnistumisen lisäksi on useita asioita, jotka voivat lisätä kuukausia tai vuosia prosessiin. Heidän joukossaan on ajoitus. Vaikka rokotekandidaatti tulisi ihanteellisesti testata aktiivisen taudinpurkauksen aikana, voi olla vaikeaa tietää missä ja milloin sellainen saattaa esiintyä.
Jopa vaikeasti kärsineillä alueilla, kuten New York City ja Wuhan, Kiina, joilla uusi taudinpurkaus näyttää olevan välitön, kansanterveysviranomaiset voivat puuttua tauteihin ehkäisemällä toimenpiteitä, kuten vaatia ihmisiä itsensä eristämiseen uudelleen. Tämä on tärkeää ihmisten terveyden pitämiseksi, mutta se voi pidentää rokotetutkimuksia koko kauden tai vuoden ajan.
Rokotehakijat putkistossa
Joulukuussa 2020 kliiniseen tutkimukseen on hyväksytty 56 rokotekandidaattia, kun taas yli 165 on prekliinisissä vaiheissa odottamassa viranomaishyväksyntää.
Testattavaksi hyväksytyistä alustoista inaktivoidut rokotteet ovat yleisimpiä. Tämä sisältää proteiini-alayksiköt, jotka käyttävät antigeenejä (komponentit, jotka stimuloivat parhaiten immuunijärjestelmää) koko viruksen sijaan, ja kokosolussa inaktivoidut rokotteet, joista joissakin käytetään "tehostavia" aineita, kuten alumiinia, vasta-ainevasteen lisäämiseksi.
RNA- ja DNA-rokotteet ovat myös hyvin edustettuina, samoin kuin vektorirokotteet, jotka käyttävät deaktivoituja kylmäviruksia rokoteaineiden kuljettamiseen suoraan soluihin.
Muita alustoja ovat viruksen kaltaiset hiukkaset, vektorirokotteet yhdistettynä antigeeniä esitteleviin soluihin ja elävä heikennetty rokote, joka käyttää heikennettyä, elävää COVID-19-muotoa stimuloimaan immuunivastetta.
(Yhdistynyt kuningaskunta)
(Kiina)
(Yhdysvallat)
(Yhdysvallat)
(Yhdysvallat)
(Kiina)
(Kiina)
(Kiina)
(Yhdysvallat)
(Kiina)
(Yhdysvallat)


.jpg)