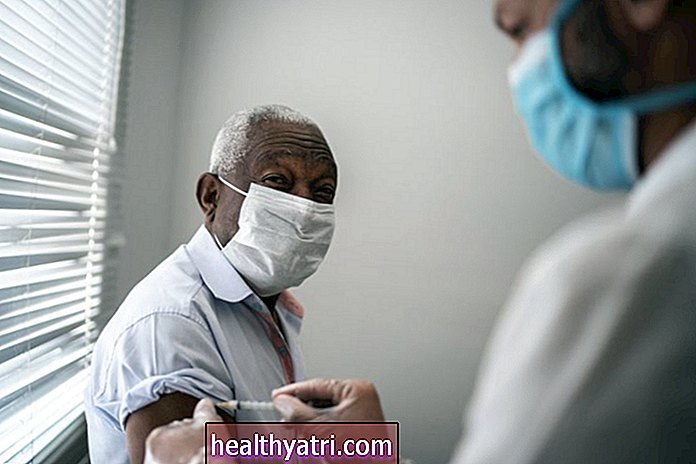
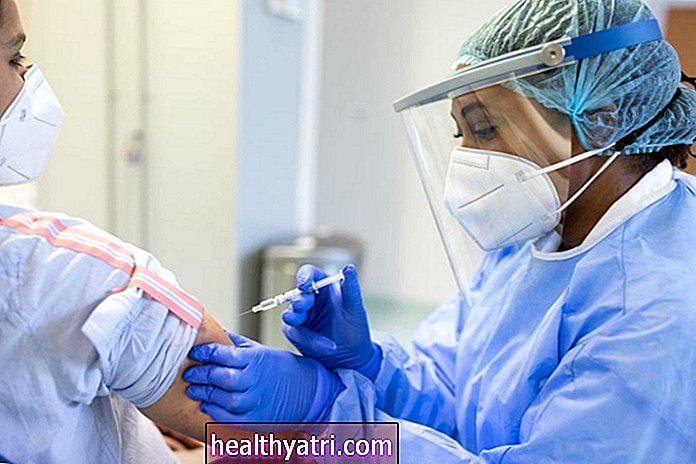
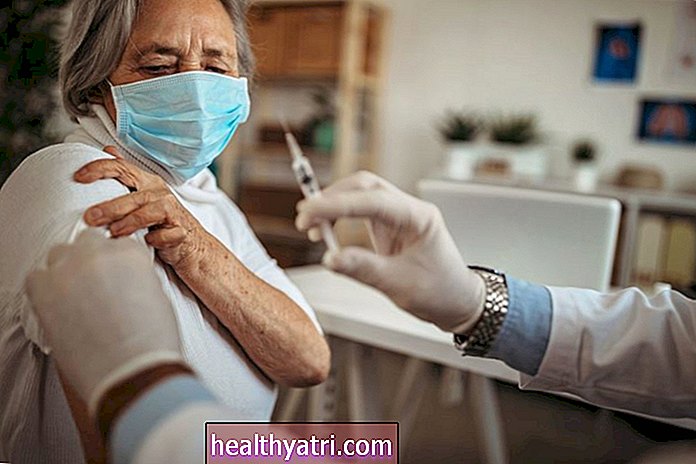
Getty Images
Tärkeimmät takeaways
- Elintarvike- ja lääkevirasto (FDA) vaatii rokotevalmistajia toimittamaan kahden kuukauden turvallisuustiedot, ennen kuin se hyväksyy COVID-19-rokotteen yleisön käyttöön.
- FDA uskoo, että kahden kuukauden jakso antaa riittävästi aikaa potentiaalisen rokotteen mahdollisille sivuvaikutuksille tai haitallisille seurauksille.
Elintarvike- ja lääkevirasto (FDA) ilmoitti 6. lokakuuta, että se vaatii COVID-19-rokotevalmistajia jakamaan kahden kuukauden turvallisuustiedot, ennen kuin se hyväksyy rokotteen käytettäväksi suurelle yleisölle. lisää yleistä epäluottamusta tulevan COVID-rokotteen turvallisuuteen.
COVID-19-rokotteet: Pysy ajan tasalla siitä, mitä rokotteita on saatavilla, kuka niitä saa ja kuinka turvallisia ne ovat.
FDA: n uudet vaatimukset
FDA: n uusien vaatimusten mukaan kliinisten tutkimusten vapaaehtoisten terveydestä on oltava kahden kuukauden seurantatiedot sen jälkeen, kun he ovat saaneet toisen rokoteannoksensa.FDA voi päättää myöntää rokotteen valmistajalle hätäkäyttöluvan - nimitys, joka sallii tuotteen julkisen käytön, jos uudet vaatimukset täyttyvät.
Shobha Swaminathan, MD
Turvallisuus on keskeisen tärkeää varmistaa, että ihmiset luottavat tekemäämme työhön.
- Shobha Swaminathan, MDFDA selitti ohjeissaan, että se haluaa nähdä tietoja vaiheen 3 kokeista, kun osallistujat ovat suorittaneet täydellisen rokotusohjelman ja kahden kuukauden ajan. FDA uskoo, että tämä aikataulu tarjoaa "riittävää tietoa rokotteen hyöty-riskiprofiilin arvioimiseksi".
Suuntaviivojen mukaan FDA tarkastelee "haittatapahtumia, vakavan COVID-19-taudin tapauksia tutkittavien keskuudessa ja tapauksia, joissa COVID-19 esiintyy aikataulussa, kun rokotteeseen sopeutuvat (eivätkä synnynnäiset) ja muistin vasteet. olisi vastuussa suojaavasta vaikutuksesta. "
FDA sanoo myös, että tutkimushenkilöiden keskuudessa on oltava riittävästi vakavia COVID-19 -tapauksia, jotta voidaan todistaa, että ihmisillä on pieni riski saada vakavia komplikaatioita rokotteesta.
Lisäksi FDA odottaa valmistajien osoittavan tietoja tietyistä oireyhtymistä - erityisesti rokotteeseen liittyvästä tehostetusta hengitystiesairaudesta (ERD) rokotteesta. "Yhteensä viisi tai useampia vakavia COVID-19 -tapauksia lumeryhmässä olisi yleensä riittää arvioimaan, tukeeko vakava COVID-19 -tapaustapa rokoteryhmän ja lumelääkeryhmän välillä suotuisan hyöty-riskiprofiilin vai päinvastoin.
Kliinisten tutkimusten vaiheessa 3 (viimeinen vaihe) on tällä hetkellä 11 rokotetta, mutta useat useiden suurten lääkeyritysten tekemät tutkimukset on viime aikoina keskeytetty sen jälkeen, kun ainakin yhdelle tutkimuksen osanottajalle on kehittynyt vakava, selittämätön sairaus.
Kahden kuukauden odotus
"Mielestäni on hienoa, että FDA vaatii, että meillä on kahden kuukauden turvallisuustiedot", tartuntatautien asiantuntija Shobha Swaminathan, apulaisprofessori ja Moderna COVID-19 -rokotustutkimuksen johtava tutkija Rutgers New Jersey Medical Schoolissa Kliininen tutkimuskeskus, kertoo Verywell. "Turvallisuus on keskeisen tärkeää varmistaa, että ihmiset luottavat tekemäämme työhön."
Swaminathan selittää, että rokotteiden yleisimmät sivuvaikutukset tapahtuvat kahden kuukauden kuluessa. ”Useimmat rokotteen haittavaikutukset, kuten kuume, uupumus ja injektiokohdan reaktiot, tapahtuvat ensimmäisen viikon aikana, ja monimutkaisempia haittavaikutuksia voi esiintyä kuuden viikon aikana. Siksi vähintään kaksi kuukautta on hyödyllistä havaita, mitä voi tapahtua. "
Shobha Swaminathan, MD
Älä siirry johtopäätöksiin tieteellisestä prosessista. Siellä on paljon väärää tietoa.
- Shobha Swaminathan, MDSwaminathan sanoo, että aikataulu "yrittää tasapainottaa julkisen tarpeen vaarantamatta turvallisuutta". Hän toivoo, että FDA: n ohje auttaa muuttamaan yleisön käsitystä rokotteiden kehittämisprosessista.
"Julkisuudessa on käsitys, että COVID-19-rokotetutkimus on kiireellistä ennen aikataulua, ja jotkut ihmiset ovat huolissaan siitä, että se tulee maksamaan turvallisuustoimenpiteitä, mikä ei todellakaan ole totta", Swaminathan sanoo. "FDA päättää, ovatko heidän [tutkijoiden] saamat turvallisuustiedot riittävät. "
Kaiken kaikkiaan Swaminathan kehottaa ihmisiä luottamaan prosessiin. "Älä siirry johtopäätöksiin tieteellisestä prosessista. Siellä on paljon väärää tietoa. "
Mitä tämä tarkoittaa sinulle
FDA: n vaatimuksen kahden kuukauden seurantatiedoista sen jälkeen, kun ihmiset ovat saaneet COVID-19-rokotteen, pitäisi auttaa varmistamaan, että mahdolliset sivuvaikutukset saadaan kiinni ennen rokotteen saatavuutta suurelle yleisölle. Prosessi voi kuitenkin lopulta kestää kauemmin.
Yleisön tulisi luottaa siihen, että rokotteiden kehittäminen ja hyväksyminen on turvallista ja että FDA ei hyväksy rokotetta ennen kuin se on valmis - ja turvallinen.